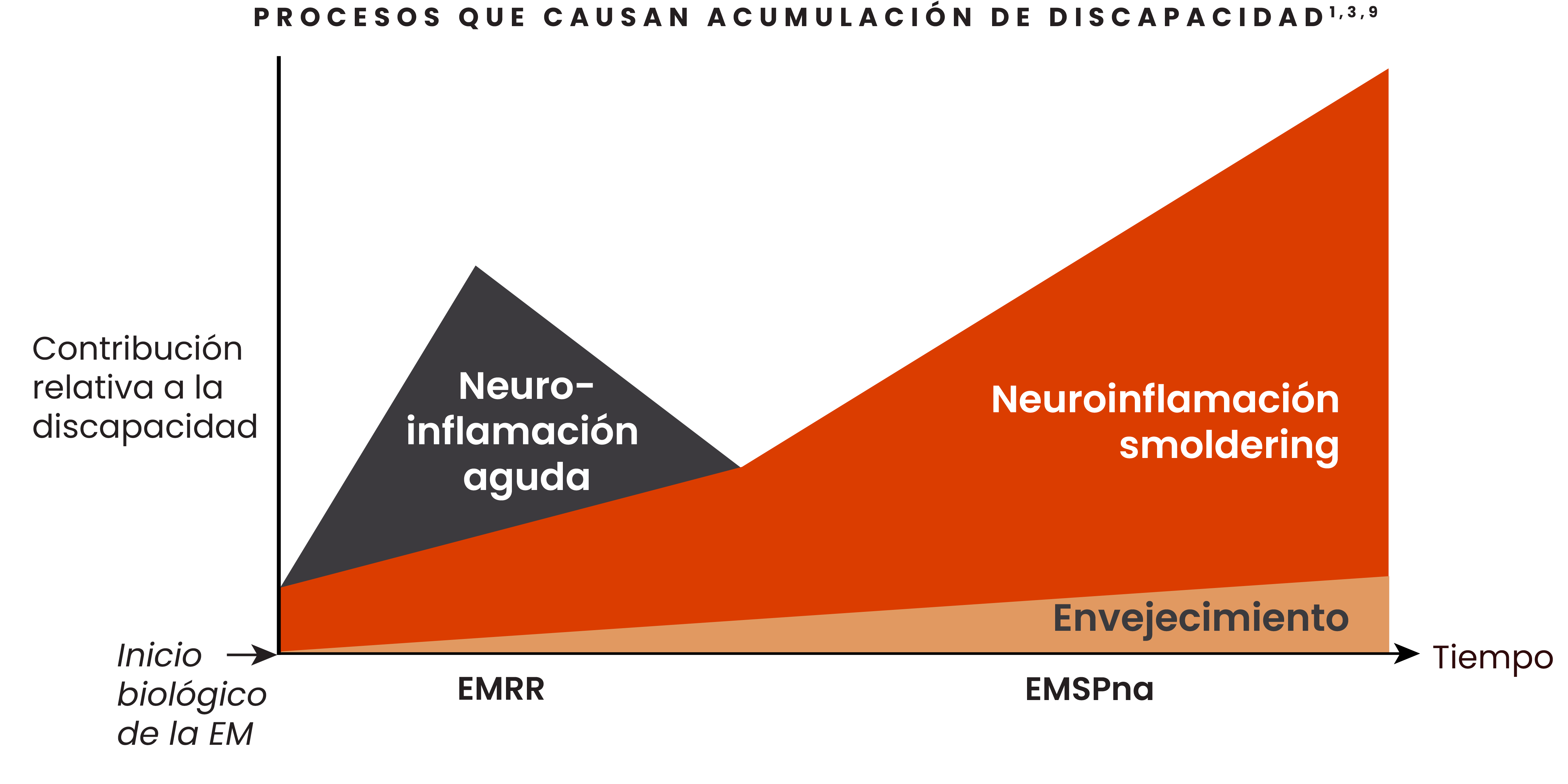
La neuroinflamación smoldering comienza a la par que el inicio de la enfermedad y es responsable del aumento gradual de la acumulación de discapacidad1,2
La contribución relativa de la neuroinflamación aguda y la neuroinflamación smoldering va cambiando a medida que los pacientes progresan de EMRR a EMSPna.1,3
Los cambios biológicos en la fase prodrómica de la EM, así como la activación microglial en el síndrome clínicamente aislado (SCA)/síndrome radiológicamente aislado (SRA), demuestran que la neuroinflamación smoldering comienza incluso antes del primer brote o lesión aguda.1,2,4-8
- Durante el curso de la EM, la neuroinflamación aguda puede disminuir, pero la neuroinflamación smoldering persiste incluso en ausencia de brotes y lesiones agudas1
- La acumulación de discapacidad causada por la neuroinflamación smoldering se puede presentar durante todo el espectro de la enfermedad9
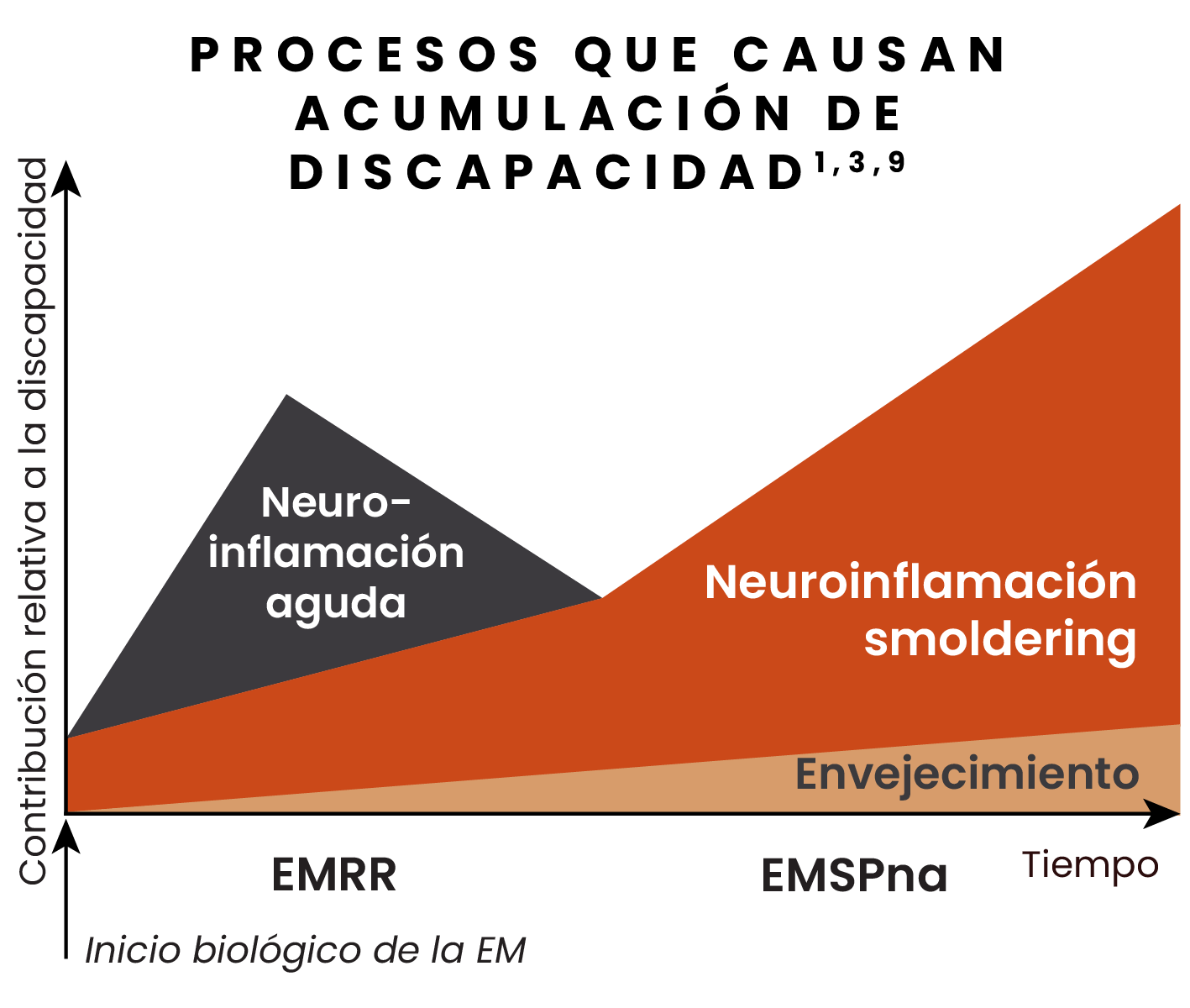
EMSPna = EM secundaria progresiva no activa; EMRR = EM remitente recurrente.
Con la creciente contribución de la neuroinflamación smoldering a la acumulación de discapacidad durante el curso de la EM, se necesitan enfoques terapéuticos específicos para abordar este proceso en todo el espectro de la enfermedad, desde la EMRR hasta la EMSPna.9
Escuche a los expertos
El Dr. Bhupendra O. Khatri, FAAN, habla del inicio de la neuroinflamación smoldering en la Reunión Anual de la AAN de 2023
Historias smoldering
La neuroinflamación smoldering podría ser la causa de la acumulación de discapacidad de Albert. Escuche su historia.
Conozca sus efectos
Sepa cómo identificar los primeros cambios físicos y cognitivos de la acumulación de discapacidad
Referencias:
-
Giovannoni G, Popescu V, Wuerfel J, et al. Smouldering multiple sclerosis: the ‘real MS’. Ther Adv Neurol Disord. 2022;15:17562864211066751. doi:10.1177/17562864211066751
-
Giovannoni G. The neurodegenerative prodrome in multiple sclerosis. Lancet Neurol. 2017;16(6):413-414.
-
Filippi M, Amato MP, Centonze D, et al. Early use of high-efficacy disease-modifying therapies makes the difference in people with multiple sclerosis: an expert opinion. J Neurol. 2022;269(10):5382-5394.
-
Absinta M, Lassmann H, Trapp BD. Mechanisms underlying progression in multiple sclerosis. Curr Opin Neurol. 2020;33(3):277-285.
-
Giannetti P, Politis M, Su P, et al. Increased PK11195-PET binding in normal-appearing white matter in clinically isolated syndrome. Brain. 2015;138(1):110-119.
-
Suthiphosuwan S, Sati P, Absinta M, et al. Paramagnetic rim sign in radiologically isolated syndrome. JAMA Neurol. 2020;77(5):653-655. doi:10.1001/jamaneurol.2020.0124
-
Bjornevik K, Munger KL, Cortese M, et al. Serum neurofilament light chain levels in patients with presymptomatic multiple sclerosis. JAMA Neurol. 2020;77(1):58-64. doi:10.1001/jamaneurol.2019.3238
-
Cortese M, Riise T, Bjørnevik K, et al. Preclinical disease activity in multiple sclerosis: a prospective study of cognitive performance prior to first symptom. Ann Neurol. 2016;80(4):616-624. doi:10.1002/ana.24769
-
Cree BAC, Hollenbach JA, Bove R, et al; University of California, San Francisco MS-Epic Team. Silent progression in disease activity-free relapsing multiple sclerosis. Ann Neurol. 2019;85(5):653-666.